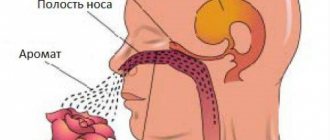
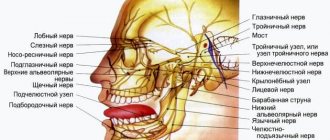
Гемифациальный спазм
— это состояние, проявляющееся безболезненными непроизвольными клоническими или тоническими сокращениями лицевой мускулатуры, иннервируемой ипсилатеральным лицевым нервом на одной стороне лица, обычно на левом. Люди не контролируют эти спазмы, которые могут продолжаться даже во время сна. Гемифациальный спазм обычно безболезнен и считается не опасным для здоровья. Гемифациальный спазм чаще встречаются у женщин среднего возраста и у азиатских людей. Это редкое состояние наблюдается примерно у 11 из 100 000 человек.
Гемифациальный спазм отличается от других нервных и мышечных состояний, поражающих лицо, потому что имеет тенденцию влиять только на одну сторону лица. Однако существуют различия между типичными для гемифациального спазма и другими формами заболевания.
Исследования показывают, что:
- 62% случаев вызваны сосудом, оказывающим давление на лицевой нерв;
- 18% имели тик, который имитировал гемифациальный спазм;
- 11% были вызваны параличом Белла;
- 6% были результатом травмы лицевого нерва;
- 2% были связаны с наследственными причинами;
- менее 1% случаев были вызваны повреждением нервов или системы кровообращения головного мозга.
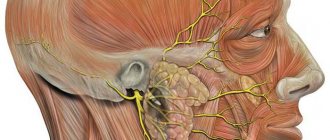
Фото: Laskawi R. The use of botulinum toxin in head and face medicine: an interdisciplinary field //Head & face medicine. – 2008. – Т. 4. – №. 1. – С. 5.
Лицевые гиперкинезы
Лицевой гемиспазм и параспазм, блефароспазм – это заболевания, связанные с неконтролируемым сокращением мышц лица. Они весьма сходны с невропатией, невритом, парезом лицевого нерва.
Управление мышцами лица построено следующим образом:
- Нервные клетки коры и подкорковых ядер головного мозга посылают нервные импульсы в ствол мозга, к центрам управления лицевым нервом;
- Эти центры распределяют импульсы по волокнам нерва и отправляют их по нерву, как по электрическому кабелю, непосредственно к мышцам лица;
- Каждое мельчайшее нервное волокно заставляет сокращаться свой микроскопический участок мышцы.
Причины лицевого гиперкинеза:
- Ошибка в работе подкорковых ядер мозга, в результате которой к мышцам лица направляются избыточные неконтролируемые нервные импульсы, которые и приводят к спазму;
- Чрезмерное возбуждение центров лицевого нерва в стволе головного мозга;
- Раздражение самого лицевого нерва уже после его выхода из мозга.
В первом и втором случаях – это результат повреждение ядра или центра при нейроинфекции, рассеянном склерозе, дефиците кровоснабжения или опухоли. В третьем случае заболевание возникает даже при незначительном сдавлении корешка лицевого нерва в области его выхода на основание мозга измененным сосудом (обвитие нерва артерией), опухолью, сдавление в толще околоушной слюнной железы при некоторых ее заболеваниях.
Даже врачи нередко путают лицевые гиперкинезы с невропатией, невритом лицевого нерва. Мы обязательно разберемся в причинах болезни и выполним необходимое лечение.
Гемифациальный лицевой спазм (ГФС) — заболевание, проявляющееся безболезненными непроизвольными односторонними тоническими или клоническими сокращениями лицевой мускулатуры, иннервируемой ипсилатеральным лицевым нервом [106, 108].
В 1875 г. F. Schultze [83] описал клинику ГФС, причиной которого являлась аневризма левой позвоночной артерии. Подробное описание клинической картины ГФС было сделано в 1894 г. французским неврологом E. Brissaud [19]. Уже в XIX веке ГФС рассматривался как отдельная нозологическая единица и выделялся из группы других лицевых гиперкинезов. За прошедшие 100 лет с момента публикации классических описаний ГФС была выявлена этиология этого заболевания и разработаны эффективные методы лечения.
В 2004 г. N. Tan и соавт. [99] продемонстрировали 203 семейным врачам видеозапись пациента, страдающего ГФС: только 9,4% из них смогли правильно поставить диагноз и 46,3% врачей смогли правильно выбрать тактику ведения такого пациента. Врачи первичного звена плохо информированы об этом заболевании, не могут назначить адекватное лечение и направить пациента к соответствующему специалисту. В современной русскоязычной научной литературе имеется ограниченное количество публикаций, посвященных диагностике и лечению ГФС [4, 9]. В современных руководствах по неврологии и нейрохирургии представления об этиологии и патогенезе отражены недостаточно полно.
В классических случаях приступ ГФС начинается с редких сокращений круговой мышцы глаза, затем, постепенно прогрессируя, спазм затрагивает всю половину лица, частота сокращения мышц нарастает и достигает такой степени, что пациент не может видеть глазом пораженной стороны (типичный ГФС). При атипичном ГФС приступ начинается с сокращения мышц щеки, далее спазм распространяется вверх по лицу [50, 80]. Приступы спазма возникают спонтанно и могут сохраняться даже во время сна, провоцируются переутомлением, стрессом, тревожным состоянием [31].
В 1905 г. невролог J. Babinski описал парадоксальную синкинезию мышц лица при ГФС: «На стороне спазма m. orbicularis oculi
сокращается, глаз закрывается, в это время внутренняя часть
m. frontalis
на стороне поражения также сокращается, что приводит к подниманию брови во время смыкания глазной щели» [15]. J. Devoize [28] назвал этот симптом «the other Babinski’s sign» («другой симптом Бабинского», чтобы отличать его от симптома Бабинского при поражении пирамидного тракта), некоторые авторы считают его патогномоничным для ГФС. Описанная синкинезия характерна для ГФС и не встречается при других лицевых гиперкинезах [90].
Впервые заболевание обычно проявляется между 40 и 50 годами жизни [14, 31]. ГФС является хроническим заболеванием, частота спонтанной ремиссии составляет менее 10% [31]. Спустя месяцы или годы после начала заболевания у пациентов может развиться умеренный парез лицевой мускулатуры на стороне поражения [51]. Слабость мышц выявляется в 47% случаев в мышцах век и в 77% при оценке силы других мышц лица [34]. Двусторонний ГФС встречается крайне редко (0,6-5%) [94, 108].
В патологический процесс могут вовлекаться другие черепные нервы. Часто ГФС сочетается с дисфункцией слухового нерва — аномалия акустического рефлекса среднего уха отмечается у 50% пациентов с гемиспазмом [71], снижение слуха в различной степени выявляется в 15% [31]. Иногда ГФС сопровождается низкотональным шумом в ипсилатеральном ухе, это связано с вовлечением в процесс m.stapedius
, которая сокращается синхронно с мускулатурой лица [84]. В 5% случаев ГФС может сочетаться с тригеминальной невралгией [63, 79, 108]. Кушинг назвал этот синдром «painful tic convulsif» — «болезненный лицевой тик». Описано сочетание ГФС с блефароспазмом [91].
По данным Миннесотского эпидемиологического исследования [14], проведенного в 1960-1984 гг., коэффициент распространенности ГФС составил 7,4 на 100 000 мужского населения и 14,5 на 100 000 женского населения; средний годовой показатель заболеваемости, стандартизированный по возрасту белого населения США на 1970 г., — 0,74 на 100 000 мужчин и 0,81 у женщин. Показатель заболеваемости и коэффициент распространенности заболевания наивысший в возрастной группе от 40 до 79 лет. Заметим, что в это исследование вошли пациенты как с первичным, так и вторичным ГФС. По данным N. Nilsen и соавт. [76], в Норвегии распространенность ГФС составляет 9,8 на 100 000 населения. Отмечена [12] более высокая заболеваемость ГФС среди лиц монголоидной расы по сравнению с европеоидами. Такие различия могут быть связаны с особенностями в строении черепа, в частности размерами задней черепной ямки [54]. Однако эпидемиологических исследований с целью выявления преобладания ГФС у лиц монголоидной расы не проводилось.
Несмотря на то что клиническая картина ГФС была описана в конце XIX века, причина этого заболевания долгие годы оставалась загадкой для исследователей. В 50-60-е годы XX века велась активная дискуссия о «периферическом» или «центральном» происхождении ГФС.
R. Siekert [86] и Э.П. Флейс [7] описали симптоматический ГФС при опухолях тимпано-югулярных гломусов. В приведенных наблюдениях обильно васкуляризированные гломусные опухоли оказывали воздействие на лицевой нерв, результатом которого явилось развитие ГФС. С.Н. Давиденков [3] и Э.П. Флейс [7] считали, что лицевой гемиспазм имеет периферическую природу, а симптомы поражения ЦНС отсутствуют. R. Wartenberg [107] изучал «центральный» генез ГФС. Cогласно его гипотезе, в основе ГФС лежат изменения функционального состояния ядра лицевого нерва и надъядерных структур. Однако все эти концепции не позволяли объяснить особенности клинической картины ГФС и разработать на их основе эффективные методы лечения.
В 1947 г. E. Camblell и C. Keedy [20], а затем E. Lain и P. Nyrac [58] выдвинули предположение, что причиной гемифациального спазма является сдавление лицевого нерва эктазированными сосудами основания головного мозга. В 1962 г. эта догадка была подтверждена при хирургической ревизии задней черепной ямки у больных с ГФС [35, 36].
Приоритет в разработке и популяризации теории микроваскулярной компрессии как причины нейроваскулярных компрессионных синдромов черепных нервов (тригеминальная невралгия, ГФС, языкоглоточная невралгия, спастическая кривошея) принадлежит американскому нейрохирургу P. Jannetta [47-49, 51]. В основе теории микроваскулярной компрессии, по его мнению, лежит нейроваскулярный конфликт — «конфликт» корешка черепного нерва в месте его входа и выхода из ствола головного мозга с прилежащим сосудом.
Основной патогенетический фактор развития синдромов микроваскулярной компрессии краниальных нервов — механическое воздействие пульсирующего сосуда на ствол нерва с последующим распространением патологической импульсации и развитием его пароксизмальной функциональной активности (пароксизмальная лицевая боль — при воздействии на тройничный нерв, пароксизмы сокращения мышц лица — при воздействии на лицевой нерв) [49]. Факторами компрессии обычно являются атеросклеротические аберрантные или эктазированные артерии. Чаще наблюдается конфликт нерва с артериальным сосудом (передней или задней нижними мозжечковыми артериями, позвоночной или базилярной артериями), редко отмечается конфликт нерва с венозным сосудом [64].
С развитием методов нейровизуализации, внедрением в широкую практику операционной микроскопии и, как следствие, улучшением техники хирургических вмешательств компрессия лицевого нерва эктазированными сосудами стала считаться основной причиной ГФС, а концепция нейроваскулярного конфликта в генезе синдромов микроваскулярной компрессии стала приобретать все большее количество сторонников [1, 2, 5, 6, 8, 29]. Согласно мнению P. Jannetta, сдавление нерва происходит в зоне входа и выхода корешка нерва (REZ — root exit/entry zone). Имеет значение, что в зоне выхода корешка более тонкий центральный глиальный миелин переходит в толстый, периферический «шванновский миелин» (впервые эта анатомическая особенность была описана H. Obersteiner и E. Redlich в 1894 г. — зона Obersteiner-Redlich) [77]).
При типичном ГФС сосуды компримируют переднекаудальную область комплекса VII/VIII нервов, а при атипичном ГФС — компрессия локализуется в заднеростральной области. Особенностями зоны нейроваскулярного конфликта объясняются отличия клинической картины типичного и атипичного ГФС [50]. Контакт сосудов с зоной выхода корешка вестибулярного нерва приводит к появлению в клинической картине жалоб на головокружение, а при контакте сосудов с зоной выхода корешка кохлеарного нерва появляются жалобы на снижение слуха и шум в ушах [50]. Возможна сочетанная компрессия корешков V и VII нервов, в этом случае ГФС будет сопровождаться лицевой болью (сочетание невралгии тройничного нерва и ГФС) [79].
Хотя общепризнанной причиной нейроваскулярного конфликта является сосудистая компрессия, опубликован ряд работ, в которых приведены данные, не укладывающиеся в классическую теорию P. Jannetta. Следует отметить, что предметом дискуссии является возможная локализация зон нейроваскулярного конфликта, а не концепция нейроваскулярной компрессии в своей основе, которая признается большинством исследователей.
H. Ryu и соавт. [81] сообщили о 7 случаях излечения ГФС после микроваскулярной декомпрессии, когда во время интраоперационной ревизии в зоне выхода корешка лицевого нерва не было выявлено факторов компрессии, а причиной спазма являлась петля передней нижней мозжечковой артерии (в 5 случаях), конфликтующая с нервом в его дистальной порции. Имеется несколько описаний [33, 72, 109] случаев выявления зоны нейроваскулярного конфликта вне зоны выхода корешка.
D. De Ridder и соавт. [27] выдвинули предположение, что частота синдромов микроваскулярной компрессии краниальных нервов в популяции зависит от длины центрального отрезка каждого из них. Поскольку наибольшую длину имеет центральный сегмент тройничного нерва [59] и далее в порядке убывания следуют лицевой, языкоглоточный и вестибулокохлеарный нервы, то соответственно чаще всего будет встречаться невралгия тройничного нерва, реже — компрессия вестибулярного нерва. Клинически значимой является компрессия нерва на всем протяжении «центрального» сегмента (покрытого «центральным» миелином отрезка нерва), а не только компрессия в зоне REZ [27]. Подобную точку зрения ранее высказывали T. Leclerq [61] и A. Moller [66].
Подтверждением этой гипотезы можно считать данные M. Sindou и соавт. [87]. Эти исследователи проанализировали результаты 579 микроваскулярных декомпрессий при невралгии тройничного нерва. Оказалось, что компрессия в зоне выхода корешка имела место только в 52,3% случаев, в его средней порции — в 54,3%, в области меккелевой полости — в 9,8%.
В настоящее время теория микроваскулярной компрессии позволяет объяснить клинические и нейрофизиологические особенности ГФС. На основе этой концепции разработан эффективный метод лечения ГФС — операция микроваскулярной декомпрессии. Этот факт, как никакой другой, свидетельствует в пользу разработанной P. Jannetta теории. Несомненно, она требует дальнейшего развития и дополнения.
Некоторые авторы полагают, что нейроваскулярный конфликт является одним из факторов в генезе ГФС и других синдромов микроваскулярной компрессии. Так, A. Kuroki и A. Moller [57] рассматривают первичную травму нерва, сопровождающуюся локальной демиелинизацией, в сочетании с сосудистой компрессией в этой зоне как сочетание пусковых факторов в развитии гемифациального спазма. Эти суждения также дополняют теорию микроваскулярной компрессии и не противоречат ей.
В некоторых исследованиях подчеркивается связь между артериальной гипертензией и ГФС. Артериальная гипертензия рассматривается как фактор риска для возникновения ГФС, так как гипертензия способствует прогрессированию атеросклеротических изменений сосудов, что приводит к их эктазии и патологической извитости, предрасполагающих развитию васкулярной компрессии. В свою очередь предполагается, что компрессия вентролатеральных отделов продолговатого мозга эктазированными сосудами может приводить к артериальной гипертензии [25, 52, 76, 93].
Развитие МРТ и МР-ангиографии позволило получить дополнительные доказательства в пользу теории нейроваскулярного конфликта, так как стала возможной прямая визуализация нервного корешка и компримирующего его сосуда. МРТ и МР-ангиография с высоким разрешением являются довольно чувствительными методами для выявления нейроваскулярного конфликта [10, 38, 92].
Иногда ГФС вызывают объемные образования мостомозжечкового угла (опухоли, сосудистые мальформации, аневризмы) [24, 100, 104]. Объемные образования изменяют нейрососудистые взаимоотношения, приводя к смещению сосудов и их контакту с нервными корешками, либо оказывают прямое компримирующее воздействие на лицевой нерв. Также причинами гемиспазма могут быть рассеянный склероз [101], лакунарный инфаркт в области моста [105], воспалительные заболевания среднего уха [60] и деформации костей черепа (например, при болезни Педжетта) [45].
Таким образом, в зависимости от этиологии можно разделить ГФС на первичный
, причинами которого является нейроваскулярный конфликт в зоне области выхода нерва из ствола, и вторичный — обусловленный другими патологическими процессами. Разделение ГФС на первичный и вторичный в настоящее время является общепринятым в литературе [22, 25, 108]. Употребление термина «идиопатический ГФС» некорректно, так как причина спазма установлена.
В настоящее время существует две основных гипотезы патогенеза ГФС. Центральная гипотеза объясняет симптоматику ГФС изменениями (гипервозбудимостью) ядра лицевого нерва [67, 68], периферическая — повреждением миелиновой оболочки и эфаптической передачи нервного импульса между различными волокнами нерва [74, 75].
V. Nielsen в 1984 г. [74, 75] выдвинул гипотезу эфаптической или эктопической передачи: в результате компрессии нерва и последующей его демиелинизации происходит формирование «ложных» синапсов, по которым эктопическая активность может запускаться вследствие механической ирритации в смежных нервных волокнах. Он показал, что в основе электрофизиологического феномена, так называемого аномального мышечного ответа при ГФС, лежит именно этот механизм. Этот феномен исчезает после декомпрессии лицевого нерва при микроваскулярной декомпрессии [51, 74, 75].
A. Moller и P. Jannetta [67-69] считают, что основные патологические процессы при ГФС происходят в ядре лицевого нерва в ответ на периферические стимулы (сосудистую компрессию). K. Digre и J. Corbett [29] выдвинули альтернативную гипотезу, согласно которой в результате компрессии в лицевом нерве происходит аберрантная регенерация, которая приводит к перестройке аксональных волокон.
В 70-80-е годы КТ и МРТ рассматривались как вспомогательные методы диагностики и служили в основном для исключения органической патологии (опухоли, сосудистые мальформации, аневризмы), которая могла вызывать вторичный ГФС, или для выявления компримирующих сосудов большого диаметра (например, эктазированной позвоночной артерии) [30, 89, 100]. С появлением высокопольных МР-томографов с высокой разрешающей способностью и последующей разработкой специального программного обеспечения (программ трехмерной реконструкции) возможности метода значительно расширились. Появилась возможность неинвазивной визуализации нейроваскулярного конфликта [10, 38, 92].
Многочисленными исследованиями показано, что МРТ и МР-ангиография с высоким разрешением являются довольно чувствительными методами для выявления нейроваскулярного конфликта [39, 92]. Y. Nagaseki и соавт. [73] продемонстрировали, что выявление сосудов небольшого диаметра (передняя и задняя нижние мозжечковые артерии) возможно в 75,9%, а сосудов большого диаметра (позвоночная артерия) — в 100%, ложноотрицательные результаты отсутствовали. Авторы подчеркивают, что диагностические возможности МРТ зависят от корректной проекции (косая сагиттальная проекция МРТ) и правильно выбранной импульсной последовательности.
На современном этапе развития МРТ в большинстве случаев позволяет выявить причину ГФС (опухоль, аневризма, сосудистая мальформация в области мостомозжечкового угла, очаг демиелинизации, очаг лакунарного инфаркта) и визуализировать нейроваскулярный конфликт, т.е. различать вторичный и первичный ГФС.
Хотя ключом к диагностике ГФС является прежде всего неврологический осмотр, электромиография (ЭМГ) также позволяет получить много полезной информации. Есть данные, что ГФС имеет патогномоничные электромиографические паттерны [32, 69]. R. Hjorth и R. Willison [43] описали два основных ЭМГ-паттерна при ГФС. Первый представляет собой короткие быстрые тики (подергивания), которые одновременно наблюдаются в различных группах мышц половины лица и часто сопровождаются мигательными движениями. На ЭМГ регистрируются изолированные залпы повторяющихся разрядов высокой частоты. Каждая серия включает от 2 до 40 разрядов от одной двигательной единицы. Интервалы между сериями разрядов в значительной степени варьируют, их частота составляет 200-250 Гц, но может достигать 350-400 Гц. Часто наблюдается затухание потенциала действия двигательной единицы во время залпа разрядов. Второй характерный, но реже встречающийся тип аномалии движений — длительные нерегулярные флюктуирующие мышечные сокращения, которые приводят к вынужденному закрыванию глаза на несколько секунд. Несмотря на то что в этой ситуации не представляется возможным зарегистрировать изолированно сигнал от отдельных двигательных единиц, исследователи смогли установить, что возбуждение двигательных единиц происходило нерегулярно и с более низкой амплитудой, чем при первом паттерне [43].
При ГФС может наблюдаться еще один электронейрофизиологический феномен: при электрической стимуляции одной из ветвей лицевого нерва происходит сокращение мышц лица, иннервируемых другими ветвями лицевого нерва, например при стимуляции височной ветви регистрируются сокращения m. mentalis
. Этот феномен получил название феномена аномального мышечного ответа (abnormal muscle response) или феномена латерального распространения (lateral spread) [67, 68]. Считается, что этот эффект обусловлен перекрестной передачей антидромной активности, возникающей вследствие микротравматизации нерва при нейроваскулярном конфликте [74, 75]. Этот феномен используется не только для диагностики ГФС, но и для интраоперационного мониторинга при выполнении МВД [39, 51, 78, 88].
ГФС следует отличать от ряда других лицевых гиперкинезов [29, 108]. R. Blair и H. Berry [18] приводят следующие заболевания и синдромы, с которыми необходимо проводить дифференциальный диагноз: эссенциальный блефароспазм; лицевая миокимия (псевдофасцикуляции), включающая тик (психогенный лицевой спазм), фокальные кортикальные судорожные приступы, затрагивающие лицевую мускулатуру, аберрантную регенерацию нервных волокон после травмы лицевого нерва или паралича Белла, отсроченную (поздняя) дискинезию (как осложнение приема нейролептиков).
К этому перечню некоторые авторы [98, 102] считают возможным относить также синдром Мейджа (сочетание блефароспазма и оромандибулярной дистонии).
Для лечения ГФС используются лекарственные препараты из разных фармакологических групп: карбамазепин [11], клоназепам [41], габапентин [23], леветирацем [26], баклофен [82]. Однако их эффект изучался на небольших выборках пациентов, без плацебо-контроля. Поэтому долгосрочный эффект такого лечения представляется достаточно сомнительным [98]. В связи с тем что при рассматриваемой патологии требуется постоянный прием медикаментов в довольно высоких дозах, необходимо учитывать их побочное седативное действие, что не может не отражаться на качестве жизни пациентов.
В лечении ГФС хорошо зарекомендовал себя ботулотоксин типа А [17, 95]. Эффективность этого лекарственного средства была установлена W. Jost и A. Kohe [53] в исследовании, проведенном с учетом принципов доказательной медицины: изучение действия ботулотоксина проводилось на больших выборках (до 2000 пациентов) в условиях двойного слепого плацебо-контролируемого исследования. Препарат вводят подкожно или внутримышечно в пораженные мышцы. Особенно перспективно использование ботулотоксина на ранних стадиях заболевания.
Однако инъекции необходимо выполнять в среднем каждые 3-4 мес [106], стоимость препарата довольно высока, кроме того, он требует строгого соблюдения правил хранения. Эффективность лечения (значительный регресс симптомов) наблюдается в 70-75% [98, 110]. В 2-14% наблюдаются такие осложнения, как птоз, кератит, диплопия, эпифора (ретенционное слезотечение), слюнотечение, страбизм (косоглазие) [53, 55]. A. Wang, J. Jancovic [106], наблюдая 110 пациентов, описали транзиторный парез мышц лица (23%), птоз (15%). Оценивая результаты лечения ботулотоксином, можно все-таки отметить их недостаточную стойкость, а высокая стоимость ограничивает его применение [78, 98].
Попытки хирургического лечения ГФС предпринимались в начале XX века. До появления методов микроваскулярной декомпрессии лечение ГФС сводилось к нанесению тяжелого или умеренного лечебного деструктивного воздействия на периферическую часть лицевого нерва или части нерва в области мостомозжечковго угла. Выполнялась полная или частичная деструкция периферической части лицевого нерва или его ветвей хирургическим путем или с помощью инъекции глицерина или этанола [40], но вместо спазма нерва иногда развивался его парез [65]. Более того, спустя 3-6 мес обычно возникал рецидив спазма вследствие регенерации нерва. Также выполнялась миоэктомия — односторонняя резекция m. orbicularis oculi
и
m. corrugator supericiliaris
[37]. В настоящее время экстракраниальные деструктивные процедуры практически не применяются в связи с их низкой эффективностью [46].
В 1960 г. W. Gardner [36] опубликовал случай излечения от ГФС после выполненного невролиза лицевого нерва в области внутреннего слухового прохода. К 1962 г. у него имелся опыт оперативного лечения 19 пациентов, всем им был выполнен невролиз VII нерва в области мостомозжечкового угла. В 7 случаях была выявлена компрессия лицевого нерва петлей передней нижней мозжечковой артерии или внутренней слуховой артерией [36]. Позднее W. Scoville [85] успешно излечил ГФС у одного пациента путем смещения периферической артерии с лицевого нерва в области мостомозжечкового угла, однако пациент утратил слух после операции.
P. Jannetta была детально разработана и популяризирована микроваскулярная декомпрессия при нейроваскулярных синдромах. Свою первую декомпрессию при ГФС он выполнил в феврале 1966 г., а в 1970 г. в свет вышла его первая статья на эту тему [47]. Операция заключается в установке протектора (обычно используется тефлон) между конфликтующим сосудом и нервом, что позволяет устранить цепь патологической импульсации. В 1999 г.
M. McLaughlin, P. Jannetta и соавт. в соответствующей публикации [64] обобщили более чем 30-летний опыт выполнения микроваскулярной декомпрессии при нейроваскулярных синдромах, приведя результаты 4400 операций.
В других научных центрах также был накоплен достаточный материал по применению микроваскулярной декомпрессии при ГФС, позволяющий утверждать, что этот метод эффективнее при лечении первичного лицевого спазма, причиной которого является нейроваскулярный конфликт, достигая 86-93% [1, 13, 16, 21, 56, 64]. F. Barker и соавт. [16] сообщили о полном регрессе симптомов ГФС у 86% пациентов из 612, частичный эффект достигнут в 5% случаев при среднем сроке наблюдения после терапии 8 лет; по отдаленным результатам, полученным R. Illingworth и соавт. [44] (средний срок наблюдения 8 лет), эффективность процедуры составила 92,2% (у 83 больных из 86).
Частота рецидивов ГФС после микроваскулярной декомпрессии, по данным разных авторов [103, 108, 109], составляет до 20%. В работе, посвященной изучению рецидивов ГФС после микроваскулярной декомпрессии, J. Tew и P. Troy [103] показали, что если у пациента после операции в течение 2 лет не возникло рецидива, то вероятность развития рекуррентного спазма составляет менее 1%, частота рецидивов в их работе приближается к 7%. Наиболее частыми осложнениями после такого вмешательства являются постоянные или преходящие нарушения функции вестибулокохлеарного и лицевого нервов. Полное выпадение функции вестибулокохлеарного нерва встречается в 1,6-2,6%, умеренное снижение слуха — в 0,6-0,7% случаев [16, 64]. Парез лицевого нерва в различных сериях встречается в 3,4-4,8%; как правило, дисфункция лицевого нерва носит преходящий характер, и при оценке отдаленных результатов микроваскулярной декомпрессии в большинстве случаев отмечается полный регресс прозопареза [78]. Во избежание нарушений функции VIII нерва используется интраоперационный мониторинг акустических стволовых вызванных потенциалов [70, 88]. Реже встречаются нарушение функции каудальной группы черепных нервов, инфекционные осложнения, раневая ликворея, кровоизлияния в ствол и мозжечок. Опубликованы работы, позволяющие оценить осложнения на больших выборках пациентов. При анализе результатов 4400 микроваскулярных декомпрессий по поводу нейроваскулярных компрессионных синдромов краниальных нервов M. McLaughlin, P. Jannetta и соавт. [64] отметили следующую частоту осложнений: в группе пациентов, оперированных до 1990 г., — повреждение мозжечка 0,87%, снижение слуха 1,98%, ликворея 2,44%. В группе пациентов, оперированных после 1990 г., количество осложнений снизилось: у 0,45% пациентов наблюдалось повреждение мозжечка, у 0,8% — снижение слуха, у 1,85% — раневая ликворея [21, 64]. Следует отметить, что у хирургов, выполняющих большое количество операций, частота осложнений сводится к минимуму [21, 64, 98].
В основе оценки результатов лечения ГФС лежит прежде всего клиническая оценка регресса симптомов гемиспазма. В связи с этим была предложена градация соответствующих изменений. Например, V. Marneffe и соавт. [62] предлагают считать результат «отличным» при полном исчезновении спазма, «хорошим» при регрессе более чем на 80%, «удовлетворительным» при регрессе от 20 до 80% и «неудовлетворительным» считается результат, если симптомы купируются менее чем на 20%. T. Iwakuma и соавт. [46], P. Jannetta [49, 51], R. Auger и соавт. [13] применяли для оценки результатов 6-уровневую шкалу, выделяя «отличный», «хороший», «удовлетворительный», «неудовлетворительный», «плохой» и «рекуррентный». Во всех системах оценки «отличным» является результат полного исчезновения симптомов, «хорошим» — исчезновение на 75-80%. Целью лечения, естественно, является достижение «отличного» или «хорошего» результатов.
Несмотря на то что ГФС не несет непосредственной угрозы жизни пациентов, он в значительной степени ухудшает ее качество, ограничивая их профессиональную и социальную активность, являясь причиной психологического дискомфорта [51, 96]. Более 75% пациентов испытывают дискомфорт из-за своего заболевания, 15-65% страдают депрессией. ГФС ухудшает зрение у 60% пациентов, препятствует выполнению трудовой деятельности у 36% больных [12].
Для оценки качества жизни пациентов с ГФС используют как «общие» (SF-36), так и специальные Hemifacial spasm шкалы (HFS-7 и HFS-8). Достоверность и надежность последних была показана в работах E.Tan и соавт. [97]. HFS-7 и HFS-8 включают 7 или 8 вопросов и очень быстро заполняются. K. Heuser и соавт. [42] продемонстрировали использование этого инструмента для оценки эффективности микроваскулярной декомпрессии при ГФС и установили, что эта процедура значительно повышает качество жизни пациентов.
Таким образом, причиной первичного ГФС является компрессия лицевого нерва в зоне выхода из ствола сосудами, вторичный ГФС чаще всего обусловлен патологическими процессами в области мостомозжечкового угла. Диагноз ГФС устанавливается клинически и с помощью данных дополнительных методов (ЭМГ, МРТ). Дифференциальный диагноз необходимо проводить с рядом других лицевых гиперкинезов. В основе современных представлений о патогенезе первичного ГФС лежит теория микроваскулярной компрессии, краеугольным камнем которой является концепция нейроваскулярного конфликта. Наиболее эффективный метод лечения первичного ГФС — микроваскулярная декомпрессия лицевого нерва. Методически данная процедура хорошо разработана. Второй по эффективности метод лечения — инъекции ботулотоксина. Этот метод имеет ряд недостатков, но ему могут отдавать предпочтение пациенты, которые категорически не приемлют для себя хирургические методы лечения. Определяющими критериями в оценке результатов лечения ГФС являются степень клинического регресса гемиспазма и улучшение качества жизни пациентов.
Обследование при гиперкинезе лица
Успех лечения напрямую зависит от точной диагностики места и причины повреждения путей и мозговых центров лицевого нерва. Поэтому мы тщательно обследуем каждого пациента. Ваш доктор установит причину избыточного возбуждения мышц лица, и на основании полученных данных подберет наиболее эффективное лечение.
МР-томография и рентгеновская компьютерная томография головного мозга и лицевого черепа. На томограммах, особенно если они выполнены с предварительным контрастированием, видны мозговые центры лицевого нерва и его область его выхода (корешок) на основание мозга, кровеносные сосуды, кости черепа. Они помогают увидеть причину сдавления корешка лицевого нерва, оценить структуру слюнных желез. Легко распознаются нарушения кровообращения, кисты и опухоли.
Анализы крови на наличие инфекций, биохимических изменений, повреждающих мозг и лицевой нерв. Подозрение на присутствие нейроинфекции и ее активность нетрудно проверить с помощью анализа крови.
Электромиография, Мигательный рефлекс – электрофизиологические методики, основанные на измерении электрических потенциалов мышц лица. Они помогают оценить функцию проведения импульсов по лицевому нерву, степень ее нарушения, судить об эффективности лечения, наличии осложнений, помогают в выборе правильной тактики лечения.
Лечение
На данный момент различают несколько способов лечения гемифациального спазма. Грамотная и своевременная терапия позволяет частично или полностью блокировать проявления данной патологии.
Медикаментозный метод
Капсулы Габапентина принимают внутрь целиком до, после либо во время еды, запивая обильно водой
Основан на приеме препаратов, относящихся к различным фармакологическим группам. Чаще всего пациентам с клоническим гемифациальным спазмом назначают такие лекарственные средства, как Клоназепам, Габапентин, Баклофен и др.
У данной методики есть довольно существенные недостатки, а потому она обычно не рассматривается в качестве серьезного лечения непроизвольных спазмов лицевых мышц. Среди минусов такого лечения следует отметить:
- Отсутствие долгосрочного эффекта.
- Большое количество побочных действий.
- Недостаточность статистических показателей.
Ботулинический токсин
Ботулотоксин вводится непосредственно в пораженную область. Согласно результатам исследований, методика показала высокую эффективность при лечении как начальных, так и запущенных стадий заболевания. Минусы методики заключаются в следующем:
- Терапия имеет высокую стоимость и требует систематического повторения.
- Если у пациента имеются проблемы офтальмологического характера, то использование препарата для них противопоказано.
- Аллергикам эта процедура также не проводится.
На данный момент лечение ботулотоксином дало положительные результаты у ¾ пациентов с лицевым гемиспазмом.
Как остановить лицевой гиперкинез. Введение Ботулотоксина А
Ботулотоксин А (Ботокс, Диспорт) – средство, позволяющее уменьшить возбудимость вовлеченной в гиперкинез мышцы.Препарат является одним из самых удобных вариантов симптоматического лечения спазмов мышц лица и глаз, и других гиперкинезов. Мы вводим Ботулотоксин А с помощью шприца с очень тонкой иглой непосредственно в пострадавшую мышцу, после чего мышца перестает включаться в тик или другой гиперкинез. Эффект развивается в течение 3-5 дней и сохраняется до 4-8 месяцев. За это время выполняется курс лечения причин заболевания и реабилитационные процедуры (массаж, гимнастика, физиолечение, психотерапия, косметологические процедуры).
Симптомы гемифациального спазма
Первым признаком спазма обычно является подергивание мышц левого века. Эти спазмы могут быть достаточно сильными, при которых происходит закрытие глаз и слезотечение. Если состояние не лечить, симптомы гемифациального спазма могут стать более серьезными и затронуть все больше и больше мышц лица. Спазм может воздействовать на мышцы рта и тянуть их в одну сторону. У некоторых людей могут развиться спазмы на обеих сторонах лица. Боль и «щелчок» в ухе, ухудшение слуха могут быть симптомами этого состояния. Иногда также возникает потеря слуха.
Лечение лицевых мышечных спазмов
В зависимости от обнаруженных причин заболевания, Ваш доктор выберет подходящую комбинацию из широкого спектра методов лечения:
- Назначение лекарственной терапии, направленной на уменьшение раздражения корешка лицевого нерва, восстановление кровоснабжения, устранение инфекции, если она выявлена;
- Введение Ботулотоксина А в мышцы, подверженные непроизвольным сокращениям;
- Иглоукалывание, массаж, гимнастика;
- Специальная нейропсихологическая гимнастика, которая позволяет нормализовать взаимоотношения между различными частями головного мозга;
- Проведение нейрохирургического вмешательства с целью устранения контакта между измененным сосудом и корешком лицевого нерва (микроваскулярная декомпрессия) или удаления опухоли.
Диагностика
Ранние случаи гемифациального спазма иногда бывает трудно отличить от миокимии лица, тиков или миоклонусов причиной, которых могут быть патологические процессы в коре головного мозга или стволе. В таких случаях, наиболее ценным диагностическим методом служит нейрофизиологическое тестирование.
Широкая и вариабельная синкинезия при тестах на моргание и высокочастотные разряды на электромиографии (ЭМГ) с соответствующими клиническими проявлениями являются диагностическими критериями гемифациального спазма. Стимуляция одной ветви лицевого нерва может распространиться и вызвать реакцию в мышце, иннервируемой другой веткой. Синкинезия отсутствует при эссенциальном блефароспазме, дистонии или эпилепсии. Игольчатая миография показывает, нерегулярные, короткие, высокочастотные всплески потенциалов (150-400 Гц) моторных единиц, которые коррелируют с клинически наблюдаемыми движениями лица.
Методы визуализации
Магнитно-резонансная томография является методом диагностического выбора, когда есть необходимость исключить компрессионное воздействие. Ангиография церебральных сосудов,как правило,имеет небольшую ценность для диагностики гемифациального спазма. Эктазированные кровеносные сосуды редко идентифицируются, и эти находки (изменения) в сосудах бывает трудно коррелировать с воздействием на нерв. Выполнение ангиографии и / или магнитно-резонансной ангиографии, как правило, применяется для выполнения хирургической сосудистой декомпрессии.
Методы диагностики
Для определения точного диагноза врачам не требуется много времени, достаточно проверить больного путем написания нескольких предложений на простой бумаге. В ходе действия можно выявить типичные симптомы аномалии:
- Неправильное расположение кисти и пальцев.
- Напряжение тонического плана, тремор, постоянное выпадение ручки и торможение процесса написания из-за болезненных ощущений.
- Компенсаторные акты (для облегчения дискомфорта пациента часто встряхивает рукой, подталкивает другую конечность или массажирует больной участок).
К наиболее востребованным диагностическим методикам относят:
- Детальный опрос и получение подробной медистории — позволяет прояснить этапы развития расстройства, вероятность повторения, присутствие неврологических аномалий.
- Неврологический осмотр — в ходе припадка выясняют тоническое состояние мышечного отдела. Долгое поражение кисти сопровождается понижением уровня мышечного тонуса до 4 из 5 баллов.
- Посещение консультации у врача-психиатра.
- Предписывается проведение электронейромиографии, которая позволит найти нарушения регуляции напряжение/вялости в отдельных группах мышц главенствующего предплечья.
- Тест письма — помогает оценить длительность и качество написанного текста.
- Магнитно-резонансное сканирование мозга — назначается для исключения онкологической опухоли, энцефалита и других серьезных заболеваний.
В чем проявляется писчий спазм?
Главным нюансом заболевания является пошаговое распространение нарушений. Процесс начинается субклиническими деформациями почерка, которые обычно игнорируются больным. В дальнейшем проявляются трудности в написании текста, возникающие при надобности быстро выполнять работу, стрессовой перегрузке, физическом напряжении. Во время прогрессирования аномалии замечаются устойчивые изменения некоторых деталей в почерке, пациент заметно медленнее пишет, начинают появляться первые проблемы. Вынужденная остановка дел происходит при резком спазме, треморе, болевом синдроме или слабости.
Чтобы предотвратить негативную ситуацию лица принимаются определенное положение рук или пальцев, делают встряхивания или подталкивания здоровой кистью, выбирают удобный предмет письма (толстый стержень для ручки, кисточки). На первом этапе развития заболевания дискинетические расстройства проявляются в изолированном характере, то есть другие виды двигательной активности (например, игра на музыкальном инструменте, вязание, использованием клавиатуру на компьютере) остаются в норме.
На поздней стадии болезни у пациента сильнее выделяются клинические симптомы, что вызывает утрату способности контролировать графоспазм волевыми усилиями, а используемые компенсаторные приемы — не работают. Нарушения прогрессируют на двигательные бытовые акты. Появляются трудности в накалывании еды столовым прибором, наборе текста с мобильного телефона, элементарном застегивании пуговиц. Врачи утверждают, что существует зависимости выраженности заболевания от позы (пациентам намного легче писать в вертикальном положении) и внешних условий. Постоянное переутомление и стрессы провоцируют стремительное развитие дисграфии, в то время как отдых и спокойствие — снижают ее проявление.
Способы лечения
Терапевтические мероприятия для пациента с диагнозом писчий спазм достаточно трудны, так как требуют регулярности выполнения, долгого времени и упорства. Медикаментозное лечение не оказывает быстрого эффекта и способны вызывать разные побочные реакции. Врачи предписывают фармакологические препараты только в комплексном курсе. Контроль за выполнением процедур выполняет невролог, реабилитолог и кинезиотерапевт. План лечения:
- Лекарственные препараты — максимальную эффективность показали комбинированные составы медсредств, которые подбираются для каждого пациента отдельно.
- Кинезиотерапия — комплекс упражнений на сохраненные движения. В некоторых случаях больному рекомендуется научиться писать другой рукой или пользоваться компьютером.
- Использование ортеза — приспособление для фиксации пальцев и руки, помогает увеличить время непрерывного письма.
- Письменные упражнения — разные методики улучшения активности.
- Ввод инъекций ботулотоксина — достаточно перспективный вариант терапии. Сложна в исполнении, так как проблематично найти конкретные очаги для ввода препарата.